绿色荧光蛋白研究进展绿色荧光蛋白研究进展
1.青岛农业大学动物科技学院,山东青岛 266109;2.中国动物卫生与流行病学中心,山东青岛 266071)
摘 要:来源于海洋多管水母属的绿色荧光蛋白(GFP)基因是目前惟一在细胞内稳定表达, 在蓝光或长紫外光的激发下,不需要任何反应底物及其他辅助因子就能发出绿色荧光的新型报告基因,无种属、组织和位置特异性,且能监测基因表达、信号转导、共转染、蛋白运输与定位,以及细胞系谱分类等。GFP对细胞无毒性,且检测方法简单,结果真实可靠,目前在多种原核和真核生物研究中得到广泛的应用。文章就GFP的生化特性、GFP的改进及其在分子生物学研究中的应用潜力进行简要阐述。
关键词:绿色荧光蛋白;选择标记基因;应用
随着生命科学和医学研究的不断深入,研究者们迫切需要一种能够在活体中表达且易于检测的报告基因,目前常用的报告基因主要有分泌型胎盘磷酸酯酶(secreted embryo alkaline phosphatase, SEAP)基因、β半乳糖苷酶(galactosidase)基因、β葡糖苷酸酶(glucosidase, GUS)基因、萤火虫荧光素酶(luciferase, LUC)基因等[1],但这些基因的检测方法并不理想,它们都需要底物和辅助因子,因而在活体中的应用受到限制。一种全新的非酶性报告基因——绿色荧光蛋白(green fluorescent protein, GFP)引起了人们的关注[2],该蛋白能够自身催化形成发色结构并在蓝光激发下发出绿色荧光。作为报告基因,GFP是能在活细胞中表达的发光蛋白;作为荧光标记分子,GFP既具有敏感的标记检测率,又没有放射性的危害。而且新的研究表明,GFP是一个良好的细胞间信号传递的动态标记分子,可以跟踪观测第二信使[3]。近来关于GFP方面的研究和综述越来越多,但多是针对某一方面的特点或应用,本文将GFP基础理论和应用做一简要综述。
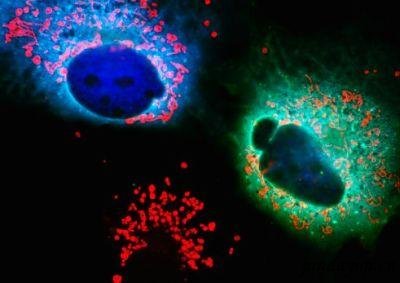
1 GFP的生化性质
1962年,Shimomura O等首次从多管水母属(Aequorea victoria)中分离纯化出了GFP,随后人们对GFP进行了广泛研究,目前研究得较为深入的是来自多管水母科(Aequorea)和海紫罗兰科(Renilla)的荧光蛋白,即AGFP和RGFP。AGFP是分子质量为27 ku~30 ku的蛋白单体,RGFP是分子质量为54 ku的同型二聚体,二者都是酸性球状蛋白质,氨基酸组成相似,发射光谱基本相同,但激发光谱不同。AGFP在395 nm和470 nm具有吸收高峰,RGFP在498 nm具有强烈的光吸收。只有完整的GFP分子才会产生生物荧光,但与荧光的产生直接有关的是GFP分子中一小段被称为色基(Chromophore)的部位。在GFP的初级氨基酸序列上,第65个至第67个氨基酸(SerTyrGly)形成环状六肽三体,以共价形式与GFP蛋白肽键骨架相连[4]。色基形成的机理目前尚不清楚,但在有分子氧存在的条件下,酪氨酸氧化成脱氢酪氨酸,并环化形成六肽,这可能是形成色基的必然过程。Shimomura O最先推导了水母GFP色基结构,后来进行了进一步验证与修改。GFP的cDNA克隆序列分析表明,在2.6 kb范围内至少分布有3个启动子,组成色基的SerTyrGly三体就位于第2个内含子3′端。
GFP用作标记蛋白,具有以下优点:①荧光稳定。GFP对光漂白有较强的耐受性,能耐受长时间的光照;GFP在pH 7~12范围内也能正常发光[5];对高温(70 ℃)、碱性、除垢剂、盐、有机溶剂和大多数普通酶(链霉蛋白酶Pronase除外)都有较强抗性。②检测方便。用荧光显微镜或肉眼就可以观察到,且可进行活体观察,不会损伤正在生长的细胞和组织[6];③无种属特异性,也没有细胞种类和位置的限制,Chalfie M等用PCR方法扩增GFP cDNA后,克隆到原核表达载体上,转化大肠埃希菌,经IPTG诱导后,在紫外光照射下转化细菌能发出绿色荧光;④GFP对受体细胞基本无毒害。Sheen J等[7]证实在玉米转GFP基因植株中,即使GFP在细胞中的表达量很高时,对细胞也不会产生明显毒害;⑤不受假阳性干扰。由于其他生物本身不含有GFP,因此不会出现假阳性结果,GFP作为分子探针可以代替荧光染料避免由于染料扩散造成的定位不准,使结果真实可靠;⑥不需任何反应底物和辅助因子;⑦可制成永久标本。GFP的荧光可以耐受光漂白,也可耐受福尔马林的固定,因而可制成长期保存的标本;⑧灵敏度高。GFP标记方法比免疫组织化学方法具有更高的灵敏度和分辨率。
尽管GFP基因作为报告基因或分子探针有许多优点,但野生型GFP发光较弱,其次荧光反应不是酶反应,不能通过添加某些物质来加强信号,且不易对荧光进行定量检测。另一方面,GFP基因在植物细胞内的表达频率并不高,甚至在某些植物细胞中并不表达。

2 GFP基因的改进
目前主要通过以下几个途径得到突变体GFP[8]:①更换GFP生色团氨基酸;②改变碱基组成;③除去GFP基因中隐蔽剪接位点;④插入植物内含子;⑤更换强启动子等突变体GFP;⑥增加荧光强度和热稳定性,促进了生色团的折叠,其荧光特性也得到了改善[9],甚至出现红色、黄绿色、蓝色等多种颜色的荧光蛋白,大大拓宽了GFP研究的领域。以下是GFP突变体的部分典型代表:①增强型GFP。Guohon S等将Ser65用Thr替代,Phe64用Leu替代,使GFP的荧光强度提高了35倍,而且激发后16 h~24 h后仍可稳定地测定荧光;②人工GFP。Zolotukhin S等改变了wtGFP基因编码区中88个密码子中的92个碱基而用人类基因组中常用的密码子代替,将GFP的荧光强度提高22倍,适合在哺乳动物细胞中高效表达;③红移荧光蛋白。将wtGFP中的Ser65用Thr替代,得到突变体。S65TGFP,激发谱中只有一个峰,且红移至490 nm,用蓝光即可激发RSFP,使之更适于普通荧光显微镜观察;④蓝色荧光蛋白。双突变体Y66H/Y145F能在381 nm光的激发下产生445 nm的蓝光,这种蓝光还能进一步激发GFP产生绿光,即发生荧光共振能量转移现象,为不同蛋白质之间及细胞器之间的相互作用研究开辟了更为广阔的视野。除以上类型的GFP突变体以外,人们还通过定点突变得到了一些可用作指示剂的GFP突变型,如pH敏感GFP,可被用来测量细胞器或更小颗粒的pH,并记录其变化,最近利用靶入了水母GFP基因的丝蛋白昆虫病毒,感染蚕的幼虫,用改造的基因取代了蚕的正常基因,当蚕吐丝时,这种丝是一种能在黑暗中发绿色荧光的纤维。
3 GFP的应用前景
GFP分子质量小,能够在异源细胞中稳定表达并发射荧光,不需要任何辅助因子参加,对细胞没有毒性,因而得到广泛应用。
3.1 作为报告基因构建基因工程载体
常用的质粒克隆载体的报告基因如LacZ,是利用酶促催化反应,需要加入外源底物和诱导物(如IPTG,Xgal),不仅操作繁琐且价格昂贵。现已构建了以GFP S65T基因作为筛选标记的新型克隆载体,建立了以绿白斑筛选法筛选阳性重组子的新方法[1011],替代LacZ蓝白斑筛选,不需Xgal,经济,简单可行。
3.2 目的基因的功能研究
将目的基因与GFP基因连接后,通过观测融合蛋白的荧光特性研究其表达和功能。哺乳动物细胞表达两种DNA拓扑酶,该酶的N末端和中部结构域序列高度保守,而其C末端结构域(Cterminaldomain,CTD)具有种属特异性。为了确定体内核定位是否仅有CTD参与就可完成,将C末端基因与GFP基因连接,并在GAL1启动子驱使下在酵母细胞中表达。通过检测GFP信号,发现两种拓扑酶的CTD均得到表达,而且拓扑酶ⅡGFP仅在细胞的有丝分裂期发现,拓扑酶ⅡGFP主要出现于细胞分裂间期,结果说明拓扑酶的CTD即足以充当核定位的信号[12]。
3.3 蛋白质缔合作用研究
Hale C A等利用GFP标记,研究了可溶性微管蛋白FtsZ与其内膜受体ZipA间的缔合作用,他们将GFP与ZipA融合,并用FtsZ与之直接结合,通过荧光检测发现,ZipAGFP融合蛋白在细胞壁缢缩前和缢缩过程中均位于FtsZ与膜相关的特殊环中,说明ZipAFtsZ的相互缔合是细胞分裂必需的。ZipA可能直接参与FtsZ环的形成和功能。
3.4 病原体与宿主关系的研究
将病原体用GFP活体标记,可以在全真条件而不是模拟条件下实时研究病原体与宿主的关系。将GFP基因插入基因组,体外转录获得感染性RNA,并以之接种烟叶,观察发现在接种点和整个植株均可表达GFP[13]。持续观察GFP的出现情况,发现整株感染时TMV以两种方式运动:①细胞间慢的传播,伴随病毒复制的GFP表达;②维管介导的快速转运,病毒不复制,GFP不表达。Barrett M等将GFP克隆于苜蓿银纹夜蛾核型多角体病毒的多角体启动子下游,发现感染24 h后在昆虫的中肠上皮细胞和血细胞中发现绿色荧光,表明在这些组织中病毒复制表达了极晚期蛋白,随后的感染发生在整个体腔的气管细胞,并进而发生在其他组织。
3.5 GFP在生态学中的应用
将GFP基因直接导入目标生物或将GFP基因克隆到病毒、细菌或质粒上,通过它们的介导而间接标记目标生物,进行生态学规律研究。用GFP基因标记遗传工程微生物以监测其在水环境中的存活和去向[14]。朱应等构建了带GFP基因的重组棉铃虫病毒。该病毒一次感染棉铃虫后不再重复感染,室内饲养3代,各代均可见典型的发绿色荧光的棉铃虫,表明病毒可以介导GFP标记其宿主,预计将为研究棉铃虫的迁飞和暴发规律提供强有力的手段。
3.6 GFP在生物防治中的应用
目前生物农药的杀虫效果往往得不到准确评估。利用GFP标记,通过荧光观察可以避免评估杀虫剂杀虫效果时仅仅记录有典型感染症状的害虫个体,而忽视无明显感染症状但确实已经感染或正在感染的害虫个体,同时无需进行分子生物学鉴定即可方便地区分杀虫剂致死和天然病原致死,从而客观准确地评价杀虫剂的毒力[15]。
3.7 GFP作为一种新型免疫标记物的探索
利用GFP的发光特性使免疫反应呈绿色荧光从而可以直接观察,可望取代传统的标记技术,建立特异、灵敏、简便和快速的免疫诊断新方法。现已将GFP基因与猪圆环病毒的特定基因相连,进行核酸定位[16],也成功地实现了GFP基因与HBVe Ag基因融合后在大肠埃希菌和昆虫细胞中高效表达,得到既能发射荧光又具有抗原性的双功能融合蛋白[17],为获得一种新型发光免疫诊断试剂奠定了基础。
4 结语
尽管GFP能在蓝光或长紫外光的激发下,不需要任何反应底物及其他辅助因子就能发出绿色荧光,但是检测GFP基因转化材料时,如果背景荧光太强,荧光信号可能被背景信号所遮盖,就很难检测到荧光信号[18]。在植物中,叶绿体和细胞壁是主要的自发荧光源,是构成检测荧光信号的主要障碍。在自发荧光较弱的情况下,通过调整光圈减少进光量或选择合适的滤光片就可以消除它们,从而突出GFP荧光。
随着分子生物学理论与技术的发展,对GFP的理论研究进一步深入,并且GFP在分子生物学领域的应用进一步加强,GFP工程,包括GFP蛋白工程和GFP基因工程的迅速发展,尤其GFP基因作为新型报告基因越来越受到关注,目前已经应用GFP作为选择标记基因成功构建多种表达外源基因的重组质粒。但是在试验过程中也发现一些因素影响着GFP的检测。另外,在细胞生物学的研究过程中发现新生GFP通过折叠和加工成为具有活性的形式过程十分缓慢。但随着生物技术的发展,对GFP的基础理论研究的进一步深入和新型突变体的不断出现,有理由相信这些问题终将得到解决,从而使GFP更好地为科学研究服务。
 QQ交谈
QQ交谈 MSN客服
MSN客服